
- 岩藻糖缺失抗体
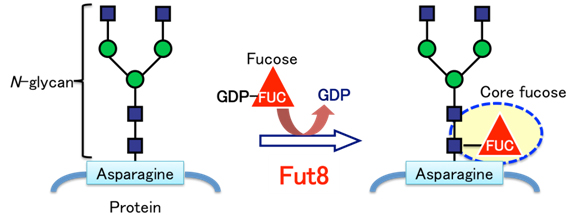
在抗体IgG的四种亚型中,目前在临床上被批准广泛使用的单克隆抗体药物主要是IgG1亚型,少量为IgG4和IgG2亚型。一个IgG1分子含有一个与抗原反应的Fab片段和一个Fc片段,在Fc片段上有在N297链接的两个双天线型的复杂的多糖链结构。 IgG1类型的抗癌抗体药物主要通过抗体介导的细胞毒作用(ADCC)、补体介导的细胞毒作用(CDC)和凋亡(apoptosis)来攻杀癌细胞。用野生型CHO细胞生产的抗癌抗体药物的Fc部分的两个双天线复杂多糖链上都带有岩藻糖(Fucose)糖基,而岩藻糖基的存在会阻碍抗体和Fc受体之间的结合,进而影响该抗体的ADCC活力和抗癌效力。研究表明[1],缺失了岩藻糖的单克隆抗体与FcRγIIIa的亲和力,比野生型单克隆抗体的亲和力有了显著的提高。Lec13突变细胞表达的无岩藻糖修饰的人IgG与FcγRIIIa亲和力提高了50倍,ADCC作用提高了100倍[2]。无核心岩藻糖使得FcγRIIIa受体中Asn162与Fc聚糖具有更高亲和力,因而结合更强。
本公司已成功开发出了自主知识产权的糖基结构改造CHO细胞株系和糖基结构改造 GS-/- CHO细胞株系,并且用这些细胞株系成功地表达和生产了多款生物仿创药物和创新型高效抗体药物。糖基结构改造CHO细胞株系和糖基结构改造GS-/- CHO细胞株系是能赋予所生产的单抗药物更高的ADCC活力的工业生产用细胞母株。本公司致力于与国内外客户的灵活商业合作,为客户提供高质量的、满足ICH药监规范的、高效稳定表达缺失岩藻糖抗体的糖基结构改造 CHO细胞株系(RCB/MCB),同时为全面提升中国生物制药业的水平贡献心力。
- 糖基结构人源化的完全缺失岩藻糖型抗体
随着越来越多的治疗性抗体在CHO细胞中的大规模量产,工程细胞株本身的特性对抗体活性的影响正日益得到业界的重视。尽管CHO细胞的糖基化与人类细胞的糖基化非常接近,但仍然有一些关键的不同之处。例如,CHO细胞表达的抗体带有大量的G0F糖型结构,少量的G1F和G2F结构,而糖链末端的唾液酸则几乎可忽略不计 。另外,有1-20%的CHO细胞来源的抗体分子带有高甘露糖(High Mannose),而人源的抗体则仅有非常痕量(<0.1%)的高甘露糖 [3]。糖链末端未被唾液酸封闭的半乳糖(Galactose)和高甘露糖对抗体的体内分布和动力学影响很大。没有唾液酸化的抗体会被肝脏中的Asialoglycoprotein Receptor(ASGPR)结合并从血液中清除。带有高甘露糖的抗体也会被肝脏中的甘露糖受体(Mannose Receptor,ManR)结合并迅速清除。据文献报道,随着末端高甘露糖含量的依次增加,不同抗体在小鼠体内的半衰期从14天到8.5天再到4.6天骤减,尽管它们对FcRn的亲和力不变 [4]。
此外,虽然CHO细胞能够进行糖蛋白的唾液酸修饰,但细胞缺乏a-2,6-sialyltransferase,因而CHO细胞产生的抗体糖链上仅带有a-2,3 位连接的唾液酸 [5]。而人类抗体糖链末端的 a-2,6 位连接的唾液酸,往往对抗体活性有重要影响。例如,血浆中提取的静脉丙种球蛋白(IVIG),其抑制炎症反应的活性主要由含a-2,6 位唾液酸,而非a-2,3位唾液酸的组分所介导 [6]。将IVIG在a-2,6 位唾液酸化后,其活性要比对照高出10倍 [7]。
安泰吉(北京)生物技术有限公司已经用基因打靶技术在CHO-K1细胞基因组中定点整合了负责人源糖基化的基因,所产生的抗体带有人类抗体的糖苷修饰。这些糖基合成途径改造过的CHO细胞株,对于开发新型抗体和高端仿制抗体,有着重要的意义。我们可用具有自主知识产权的CHO改造细胞株,为客户定制表达糖基改造的抗体。







